Tantal je speciální druh kovu, který patří do ušlechtilé skupiny. Byl objeven již v roce 1802, ale je považován za mladý prvek. I přes svou vzácnost má široké využití nejen ve šperkařství, ale i v průmyslu. Obvyklá je zejména v elektronice – obsahuje ji téměř každé zařízení.
Masové používání tohoto kovu začalo ve 40. letech minulého století a trvá dodnes. Svou oblibu si získal díky zvýšeným pevnostním vlastnostem. Kromě toho má mnoho jedinečných fyzikálních a chemických vlastností.
Fyzikální a chemické vlastnosti
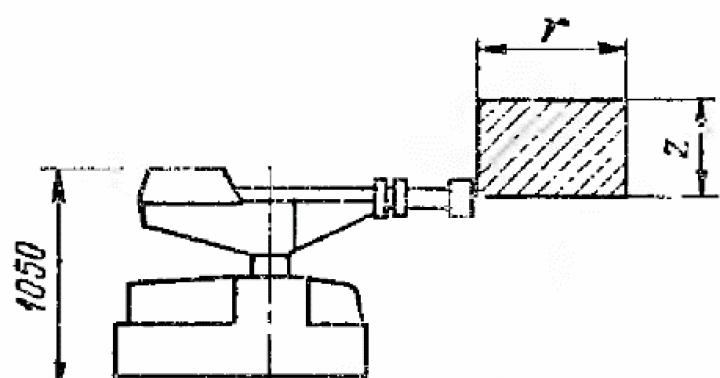
Z fyzikálních vlastností tohoto kovu je třeba vyzdvihnout vysoký bod tání, který je 3017 stupňů Celsia, což jej odlišuje od mnoha analogů. Díky tomu se používá v oblastech, kde je vyžadována zvýšená odolnost vůči extrémním podmínkám. Mezi vlastnosti tantalu zároveň patří tažnost a tvrdost, jejichž kombinace je v přírodě poměrně vzácná.
Teplota tání tantalu je 3017 °C.
Výše uvedené vlastnosti tantalu umožňují opracovat kov bez větší námahy a vytvořit požadované tvary a velikosti. Speciální struktura atomu je velmi důležitá pro vytváření částí a mechanismů struktur se zvýšenou odpovědností. Tantal se dobře hodí ke kování a válcování. V tomto případě lze s úspěchem použít i metodu deformace za studena. Je třeba zdůraznit vysokou tepelnou vodivost.
Díky své vysoké hustotě lze kov použít k výrobě malých ozubených kol a částí elektrických spotřebičů, které jsou odolné proti opotřebení a neznehodnocují se po dlouhé době používání.
V některých případech se používá jako pohlcovač plynu. Je třeba zdůraznit elektronickou konfiguraci: kov má v normálním stavu a při vysokých teplotách odlišné vlastnosti elektrické vodivosti.
Tantalové díly lze spojovat pájením, svařováním nebo nýtováním. Nejčastěji se používá metoda svařování, protože kvalita svaru se vyznačuje vysokou pevností a odolností vůči fyzickému namáhání.
Z chemických vlastností stojí za vyzdvihnutí jeho vysoká odolnost vůči oxidaci a zásadám. Po roztavení je však částečně citlivý na alkálie. Oxidace je nemožná při teplotách pod 250 stupňů.
Chemické vlastnosti tohoto kovu jsou velmi podobné sklu. Je téměř nemožné ji rozpustit v kyselině, pokud nepoužíváte kyselinu fluorovodíkovou a dusičnou. Dokonce i vystavení kyselině sírové neovlivňuje strukturu a tvar kovu. Na povrchu se může objevit pouze malý film. Rovněž nepodléhá zničení při dlouhodobém vystavení mořské vodě.
Výskyt v přírodě a výroba tantalu
Tantal je jako chemický prvek v přírodě velmi vzácný, tvoří pouze 0,0002 % zemské kůry. Velmi zřídka se vyskytuje v čisté formě, nejčastěji ve složení různých minerálů, v blízkosti jiného kovu - niobu.
Ložiska tohoto prvku se nacházejí v mnoha zemích. Velká ložiska se nacházejí ve Francii, Egyptě, Číně a Thajsku. Ale největší ložiska tohoto prvku jsou v Austrálii. Tantal se těží v množství více než 400 tun ročně. Potřeba jeho využití přitom neustále roste, s čímž souvisí i nárůst objemu elektrozařízení vyrobených za použití tohoto kovu. Na základě toho dochází k neustálému rozvoji nových ložisek.
V naší zemi je výroba tantalu soustředěna v hořčíkovém závodě Solikamsk. Kov se získává zpracováním koncentrátů loparitu. V jiných zemích se používají i jiné minerály, jako je rutil, struverit, tantalit a kolumbit.
Největšími producenty tohoto kovu na světě jsou USA, Japonsko a Čína. Počet světových výrobců nepřesahuje 40 firem. Cena - od 1000 dolarů za kg.
Slitiny na bázi tantalu
Pro své speciální fyzikální vlastnosti je tento kov ve své čisté formě velmi často využíván v průmyslu. Pro zvýšení pevnosti a odolnosti vůči vysokým teplotám však lze použít slitiny na jeho bázi a přidat vhodné legovací složky.
Slitiny tantalu mohou zůstat pevné při teplotách kolem 1700 stupňů. To je nezbytné při použití sloučenin tantalu v energetice, chemickém průmyslu, výrobě vysoce přesných nástrojů a metalurgii. Velmi často se při konstrukci vesmírných raket používají různé slitiny.
Typ použitých legujících složek závisí na požadovaných konečných vlastnostech. Pro zlepšení kvality práce se používají prvky, které dávají slitině zlepšené vlastnosti tažnosti.
Je třeba poznamenat, že velmi často se tantal ve slitinách nepoužívá jako základ, ale jako legující složka. Jeho přidání do různých materiálů umožňuje zvýšenou odolnost vůči vysokým teplotám a korozi.
Obvod tantalového kondenzátoru
Tantal TAV-10 je široce používaná slitina na bázi tohoto kovu. Vyrábí se s přídavkem wolframu, jehož množství je asi 10%. Výsledkem je materiál se zlepšenou tepelnou odolností. Používá se k výrobě topných těles a pro lékařské účely, protože jeho složky nedráždí lidskou pokožku.
Aplikace tantalu
Použití tantalu není omezeno na jednu oblast. Stojí za to zdůraznit oblasti, ve kterých se tantalové produkty nejvíce používají:
- Hutnictví. Téměř polovina tohoto kovu se používá v metalurgickém průmyslu. To je způsobeno tím, že se snadno používá k vytváření různých slitin, zejména antikorozních ocelí, které jsou odolné vůči vysokým teplotám. Tantalový drát se používá v různých oblastech, kde je vyžadována zvýšená pevnost a tepelná odolnost. Karbid tantalu je také široce používán při výrobě kelímků pro žáruvzdorné kovy.
- Elektrotechnika. Asi 25 % se využívá při výrobě elektrotechniky a elektrospotřebičů. Kondenzátory využívající tento prvek se vyznačují zvýšenou provozní stabilitou. Navíc v případě zničení povrchu kondenzátoru se vytvoří film oxidu tantalu, který jej chrání. Vyzdvihnout byste měli také prvky, jako jsou anody, katody, lampy a další kovové díly, které jsou na jeho základě také vyráběny.
- Chemický průmysl. Pětina vyrobeného objemu se využívá v chemickém průmyslu. Je to dáno tím, že je odolný vůči většině kyselin, solí a zásad.
- Lék. Tantal v lékařství se používá v takových odvětvích, jako je kostní a plastická chirurgie. Prvky vyrobené z tohoto materiálu se používají k upevnění kostí pro dosažení zvýšené pevnosti bez podráždění organické tkáně.
- Vojenská sféra. Ve vojenské sféře se vyrábí tantalové terče a nábojnice pro kumulativní projektily.
- Instrumentace. Tento kov se používá k výrobě přesných přístrojů, kontrolních zařízení a různých membrán, jakož i vakuových přístrojů, protože se vyznačuje svými vlastnostmi absorpce plynů.
- Nukleární energie. V této oblasti působí kov jako výměník tepla.
Je třeba poznamenat, že rozsah použití tantalu je omezen pouze malým objemem jeho výroby. Pokud se objem výroby zvýší, rozsah použití se výrazně rozšíří.
Tantal- světle šedý kov s lehce namodralým nádechem. Z hlediska žáruvzdornosti (bod tání asi 3000 °C) je na druhém místě za wolframem a rhenium. Vysoká pevnost a tvrdost se snoubí s vynikajícími plastovými vlastnostmi. Čistý tantal se dobře hodí k různému mechanickému zpracování, snadno se lisuje, zpracovává na nejtenčí plechy (asi 0,04 mm tlusté) a drát.
Tantal má kubickou mřížku centrovanou na tělo (a = 3,296 Å); atomový poloměr 1,46 Á, iontové poloměry Ta 2+ 0,88 Á, Ta 5+ 0,66 Á; hustota 16,6 g/cm3 při 20 °C; tpl 2996 °C; teplota kipu 5300 °C; měrná tepelná kapacita při 0-100°C 0,142 kJ/(kg K); tepelná vodivost při 20-100 °C 54,47 W/(m K). Teplotní koeficient lineární roztažnosti 8,0·10 -6 (20-1500 °C); měrný elektrický odpor při 0 °C 13,2·10 -8 ohm·m, při 2000 °С 87·10 -8 ohm·m.
Při 4,38 K se stává supravodičem. Tantal je paramagnetický, specifická magnetická susceptibilita 0,849·10 -6 (18 °C). Čistý tantal je tažný kov, který lze zpracovat tlakem za studena bez výrazného kalení. Lze jej deformovat s mírou redukce 99 % bez mezižíhání. Přechod tantalu z tvárného do křehkého stavu po ochlazení na -196 °C nebyl zjištěn.
Modul pružnosti tantalu je 190 H/m2 (190-102 kgf/mm2) při 25 °C. Pevnost v tahu žíhaného tantalu vysoké čistoty je 206 MN/m2 (20,6 kgf/mm2) při 27 °C a 190 MN/m2 (19 kgf/mm2) při 490 °C; relativní prodloužení 36 % (27 °C) a 20 % (490 °C). Tvrdost čistého rekrystalizovaného tantalu podle Brinella je 500 Mn/m2 (50 kgf/mm2). Vlastnosti tantalu závisí do značné míry na jeho čistotě; nečistoty vodíku, dusíku, kyslíku a uhlíku činí kov křehkým.
Chytrý kov. Tento termín se objevil v obchodním světě v polovině 20. století. Inteligentní kovy byly použity jako high-tech materiály používané v elektronice a robotice. Tantal se stal jedním z těchto high-tech kovů. Dnes je neoddělitelně spojen s takovými pojmy, jako jsou satelitní komunikace, palubní systémy a telekomunikační zařízení.
Co je tantal? Historická fakta
Tantal byl poprvé objeven v roce 1802 švédským vědcem A.G. Ekeberg ve složení dvou minerálů nalezených ve Švédsku a Finsku. Oxid tohoto prvku byl velmi stabilní a ani velké množství kyseliny nemohlo zničit jeho strukturu. Vědec vytvořil dojem, že kov nemůže být nasycen kyselinou. Ekeberg si vzpomněl na legendu o králi Tantalovi, který byl synem Dia a v důsledku trestu nemohl uhasit hlad a žízeň. Jeho utrpení se nazývalo tantalová muka.
Stejně tak vědec, ať se snažil sebevíc, nedokázal izolovat čistý kov od oxidu, a tak svou práci porovnal s tantalovou moukou. Chemickému prvku dal jméno tantal a minerál, který tento kov obsahoval, nazval tantalit. Teprve v roce 1903 Němec Bolton V. získal tažný kov tantal v jeho čisté formě. Jeho průmyslová výroba začala až v roce 1922. První příklad průmyslové výroby tantalu měl pouze velikost hlavičky zápalky. Jako první jej začaly vyrábět Spojené státy a v roce 1942 byl spuštěn závod na výrobu tohoto kovu.
Fyzikální vlastnosti tantalu
Co je tantal? stříbrno-bílá barva. Odolný oxidový film na něm dodává podobný vzhled jako olovo. Kov má vysokou pevnost a tvrdost a zároveň tažnost. Svou tažností je přirovnáván ke zlatu.

Ve své čisté podobě dokonale podléhá mechanickému zpracování. Snadno se razí a vyroluje do velmi tenké vrstvy do 0,04 mm. Vyrábí vysoce kvalitní drát. Tantal, co to je? Je to žáruvzdorný kov, jehož bod tání je přibližně 3000 stupňů. V této vlastnosti jej předčí pouze wolfram a rhenium. Jednou z jeho specifických vlastností je vysoká tepelná vodivost. Ani oxidový film, který se na něm tvoří, tuto vlastnost nesnižuje.
Chemické vlastnosti
Mnoho organických a anorganických kyselin - chloristá, sírová, chlorovodíková, dusičná a další agresivní prostředí - nezpůsobuje korozi tantalu. Kov při zahřátí z 200 na 300 stupňů oxiduje a pod oxidovým filmem se vytvoří plynem nasycená vrstva. Slabé chemické vlastnosti tantalu nedovolují, aby se rozpustil ani v aqua regia, která taví platinu a zlato.

V praxi se prokázalo, že nerezové oceli jsou při provozu méně odolné a díly z nich mají výrazně kratší životnost než výrobky z tantalu. Ze všech existujících kyselin dokáže tento kov rozpustit pouze kyselina fluorovodíková.
Slitiny
Silná odolnost tantalu vůči kyselinám umožňuje jeho použití jako přísady do různých slitin používaných při výrobě kovových konstrukcí. Pro výrobu válcovaných výrobků - drátů, pásů, plechů, trubek - se používá slitina tantalu a hafnia. wolfram a tantal se používají k výrobě břitových destiček pro různé účely. Takové slitiny se vyznačují:
- vysoká síla;
- zvýšená tvrdost;
- neoxidují;
- mají vysokou odolnost proti otěru;
- jsou odolné proti opotřebení;
- mají významnou viskozitu;
- poskytují vynikající pevnost řezné hraně nástroje.
Slitina tantal-wolfram, která obsahuje 7 % wolframu, odolává teplotám až 1900 stupňů. Mezi odborníky vzbuzuje značný zájem. A trysky pro raketové motory jsou vyrobeny ze slitiny tantalu s 10% wolframu. V kosmické technice se používají materiály, které mají dobrou tepelnou kapacitu nebo žáruvzdornost, proto se pro jeho výrobu široce používají slitiny tantalu.
Role šrotu
Tantalový šrot tvoří významný podíl, až 30 % tržních dodávek, z celkového objemu. Většina kovu pochází z odpadních kondenzátorů. Proto je jeho dodávka přímo závislá na činnosti v elektronickém průmyslu.

A to je zase určeno globálními ekonomickými podmínkami. Dalšími zdroji šrotu jsou použité karbidy. Slitiny šrotu, jejichž hlavním prvkem je nikl, obsahují také tantal. V budoucnu bude důležitým zdrojem tohoto kovu spotřební odpad.
Použití tantalu
Samotný kov a jeho slitiny jsou široce používány v průmyslu. Používá se k výrobě:
- suché elektrolytické kondenzátory;
- ohřívače pro vakuové pece;
- nepřímé topné katody;
- antikorozní zařízení;
- jaderné reaktory;
- supravodiče;
- střelivo se zvýšenou průbojností;
- hmotnostní standardy, které mají vysokou přesnost;
- řezné nástroje s vysokou životností.
Vysoká odolnost kovu vůči korozi pomáhá prodloužit životnost tantalových kondenzátorů v elektronických systémech až na 12 let.

Klenotnický průmysl používá tento kov k výrobě pouzder hodinek a náramků místo platiny. Výrobky z tantalu se používají také v lékařském průmyslu. Lidské tělo ho neodmítá, proto se používá k výrobě:
- destičky na lebky a břišní dutinu;
- kancelářské sponky, které se používají ke spojování nádob;
- silné nitě, které nahrazují šlachy;
- tenké nitě pro sešívání nervových vláken.
GOST kov
Existuje několik metod pro stanovení norem GOST pro tantal a jeho oxidy, například fotometrické a spektrální.
Spektrální metoda (GOST 18904.8) určuje obsah nečistot vápníku, wolframu, mědi, kobaltu, sodíku a molybdenu v tantalu a jeho oxidu. Výsledkem analýzy je aritmetický průměr získaný ze 2 stanovení různých vzorků.
Fotometrická metoda (GOST 18904.1) stanovuje obsah hmotnostního zlomku wolframu a molybdenu v tantalu a oxidu. V tomto případě se výsledek analýzy vypočítá jako aritmetický průměr 3 stanovení, která se provádějí ze samostatných vzorků.
Ložiska a těžba tantalu
Co je tantal? Jedná se o velmi vzácný kov. Ve své čisté formě se prakticky nepozoruje. Nachází se v minerálech a ve formě vlastních sloučenin. V minerálech se vždy nachází společně s niobem, který je svými vlastnostmi velmi podobný tantalu. Ložiska se sloučeninami a minerály tantalu se nacházejí v mnoha zemích světa.

Největší se nachází ve Francii. Zásoby tohoto kovu jsou vysoké v Číně a Thajsku. V zemích SNS jsou vklady mnohem menší. Ročně se na světě vyrobí asi 420 tun tantalu. Hlavní závody zpracovávající kov se nacházejí v Německu a USA. Vzhledem k prudkému rozvoji elektroniky, ve které není použití tantalu nejméně důležité, je tohoto vzácného kovu nedostatek, což vede k hledání nových ložisek.
Ceny tantalu
Většina tantalu, a to až 60 %, se jeho použitím spotřebuje asi na 20 %. Ceny tohoto vzácného kovu se mohou rychle měnit. Poptávka po něm se buď obnoví, nebo znovu klesne. Analytici předpokládají, že nabídka a poptávka budou v příštích letech kolísat, zejména v závislosti na ekonomických faktorech.
Přibližná cena tantalu za 1 kg v rublech na ruském trhu je:
- list - 65 660;
- v prutech - 73 030;
- drát - 73 700.
Vyhlídky
Stále více lidí začíná tento chytrý kov využívat v lékařském průmyslu pro potřeby rekonstrukční chirurgie. Používá se k výrobě implantátů. Tantalová příze se používá k náhradě svalové tkáně, drát se používá k upevnění kostí a nitě se používají k šití. Díky zásadnímu převybavování světových aerolinek pro potřeby leteckého průmyslu bude dále růst. Slitiny v leteckém průmyslu se používají pro letecké motory. Kromě toho se tantal nadále aktivně používá pro výrobu počítačového vybavení: procesory, tiskárny.

Poptávka po tomto kovu neklesá ani v chemickém průmyslu. Je široce používán pro výrobu chlóru, peroxidu vodíku a mnoha kyselin. Chemické inženýrství jej široce využívá při výrobě zařízení v kontaktu s agresivním prostředím. Nejvážnějším spotřebitelem tantalových slitin zůstává metalurgický průmysl. Poptávka po něm roste i v jaderné energetice, kde se využívá především tepelná vodivost v kombinaci s tažností a tvrdostí tantalu.
Kovový tantal otevřen poměrně nedávno, konkrétně v roce 1802. Švédský chemik A.G. měl to štěstí, že objevil tento kov. Ekeberg. Při studiu dvou nových minerálů, které byly nalezeny ve skandinávských zemích, se ukázalo, že kromě známých prvků obsahovaly i ty dříve neprozkoumané. Vědec nikdy nebyl schopen izolovat kov z minerálu v jeho čisté formě, protože s tím vyvstaly velké potíže.
V tomto ohledu byl neprozkoumaný kov pojmenován po hrdinovi z mytologie starověkého Řecka a podle kterého byl napsán mýtus o Tantalovi. Po tomto, více než 40 let, se tomu věřilo tantal a niob- jedná se o stejný kov. Jeden německý chemik však prokázal rozdíl mezi kovy a poté další Němec izoloval tantal v jeho čisté formě, a to se stalo až v roce 1903.
Sériová výroba válcovaných výrobků a tantalové výrobky začala teprve během druhé světové války. Dnes se tomuto prvku říká „chytrý kov“, protože rychle se rozvíjející elektronika se bez něj neobejde.
Popis a vlastnosti tantalu
Tantal je kov s vysokou tvrdostí a atomovou hustotou. V periodických chemických prvcích se tantal nachází na pozici 73. Ve světové praxi je zvykem označovat tento kov kombinací dvou písmen, a to Ta. Při atmosférickém tlaku a pokojové teplotě má tantal charakteristickou stříbřitě kovovou barvu. Oxidový film, který se tvoří na povrchu kovu, mu dodá olovnatý odstín.
Tantalový prvek neaktivní při pokojové teplotě. Oxidace povrchu tohoto kovu vzduchem je možná pouze při teplotách nad 280 stupňů. Tantal reaguje s halogeny při teplotě o 30 stupňů nižší než se vzduchem. V tomto případě se na povrchu vytvoří ochranný film, který zabraňuje dalšímu pronikání oxidačních prvků do celé hloubky kovu.

Chemický prvek tantal s poměrně vysokým bodem tání. Je to tedy 3290 K a bod varu dosahuje 5731 K. Navzdory vysoké hustotě (16,7 g/cm3) a tvrdosti je docela plastický. Z hlediska tažnosti lze tantal srovnávat s. S čistým kovem se velmi snadno a pohodlně pracuje.
Snadno se opracovává, lze jej například vyválcovat na tloušťku 1-10 mikronů. Je třeba také poznamenat, že tantal je paramagnetický. Zajímavá vlastnost tohoto kovu se začíná objevovat při teplotě 800 stupňů: tantal absorbuje 740 svých plynových objemů.
Ve světové praxi již existuje řada faktů, které svědčí o vynikající odolnosti tohoto kovu ve velmi agresivním prostředí. Například je známo, že tantalu nepoškodí ani 70% kyselina dusičná. Kyselina sírová do 150 stupňů také nevede ke korozivnímu rozkladu, ale již při 200 stupních se kov začne rozpouštět rychlostí 0,006 mm/rok.
Některá výrobní fakta také naznačují, že tantal je mnohem odolnější než austenitické nerezové oceli. Proto je znám případ, kdy tantalové díly vydržel o 20 let déle než díly z nerezové oceli.

Další zajímavostí je, že tantal se používá ke katalytické separaci zlata. Vyrábějí se z něj katody, na které se ušlechtilý kov nanáší a poté se smyje aqua regia. Katoda a tantal přitom zůstávají díky své vynikající odolnosti vůči kyselinám nedotčené.
Aplikace tantalu
Kdysi se tento kov používal k výrobě vláken v žárovkách. Dnes tantal a slitiny tantalu používá se v následujících odvětvích a produktech:
— při tavení žáruvzdorných a korozivzdorných slitin (například součástí leteckých motorů);
— v chemickém průmyslu vytvářet zařízení odolná proti korozi;
— v hutní výrobě pro výrobu kovů vzácných zemin;
— při stavbě jaderných reaktorů (tantal je nejodolnější kov vůči parám cesia);
— díky své vysoké biokompatibilitě se tantal používá k výrobě lékařských implantátů a protéz;
- na výrobu supravodičů - kryotronů (jedná se o prvky výpočetní techniky);
- používá se ve vojenském průmyslu k výrobě nábojů. Použití tohoto kovu zvyšuje průbojnou sílu munice;
- účinnější nízkonapěťové kondenzátory jsou vyrobeny z tantalu;
- V poslední době se tantal v podnikání pevně usadil. To je způsobeno schopností kovu vytvářet na povrchu silné oxidové filmy, které mohou mít různé barvy a odstíny;
- velký počet modifikace tantalu se hromadí v jaderných reaktorech. Pro laboratorní nebo vojenské účely lze tuto modifikaci kovu použít jako zdroj gama záření;
— tento kov se používá jako hlavní (po platině) pro výrobu hmotnostních etalonů, které mají zvýšenou přesnost;
- nějaké intermetalické sloučeniny tantalu mají velmi vysokou tvrdost a pevnost, stejně jako zvýšenou odolnost proti oxidaci. Tyto sloučeniny se používají v leteckém a kosmickém průmyslu;
— karbidy tantalu se používají k výrobě řezných nástrojů se zvýšenou odolností vůči červenému. Nástroj se získává slinováním směsi karbidových prášků. Tyto nástroje se používají ve velmi obtížných podmínkách, například při příklepovém vrtání;
- pětimocný oxid tantalu nezbytné pro svařování skla v jaderné technologii.
Ložiska a těžba tantalu
Tantal je vzácný kov. Jeho množství v zemské kůře je pouze 0,0002 %. Toto množství zahrnuje dvě modifikace kovu: stabilní a radioaktivní. Tento vzácný kov se vyskytuje ve formě vlastních sloučenin a je součástí mnoha minerálů. Pokud je tantal obsažen v minerálu, bude vždy spolu s niobem.

Ložiska sloučenin tantalu a minerály se nacházejí v mnoha zemích. Největší naleziště tohoto prvku v Evropě se nachází ve Francii. Na africkém kontinentu má nejvíce tantalu Egypt. Vysoké zásoby tohoto kovu má také Čína a Thajsko. Menší ložiska se nacházejí v SNS, Nigérii, Kanadě, Austrálii a dalších zemích. Největší dosud objevená ložiska jsou však v Austrálii.
Ročně se na světě vytěží asi 420 tun tantalu. Hlavní zpracovatelské závody tohoto kovu se nacházejí v USA a Německu. Stojí za zmínku, že mezinárodní společenství deklaruje potřebu zvýšit produkci tohoto vzácného kovu. Taková prohlášení souvisejí především s nárůstem výroby elektroniky, ve které je tento prvek intenzivně využíván.

Rozvinutých oborů tak každým rokem přibývá. Například k hlavním světovým rozvojovým oborům přibyla další místa v Brazílii, USA a Jižní Africe. Je však třeba poznamenat, že v posledních 10 letech došlo k intenzivnímu snížení produkce tantalu. Nejnižší produkce v 21. století byla zaznamenána v roce 2010.
Cena tantalu
Cena tantalu za posledních 15 let značně kolísala. Takže v letech 2002-2003 koupit tantal bylo to možné za nejnižší cenu. Tento rok cena tantalu se pohybovala od 340 do 375 dolarů za kilogram. V Rusku dnes můžete koupit tantal, cena což je 2950 rublů za kilogram.
Rozdíl ve vlastnostech tantalu ve formě kousků a prášku je tak velký, že se zdá, jako by šlo o dva různé kovy. Při zahřátí prášek velmi intenzivně interaguje s kyslíkem (280 °C):
4Ta+5O2 = 2Ta2O5,
s halogeny (250 - 300 °C):
2Ta + 5Cl2 = 2TaCl5,
a dokonce i s dusíkem (při zahřátí na 600 °C v proudu dusíku):
Tantalový kov je stabilní v naprosté většině agresivních prostředí. Žádné kyseliny a dokonce ani aqua regia to neovlivňují. Jedinou výjimkou je kyselina fluorovodíková H2F2, ale to je způsobeno přítomností fluorového iontu v ní. I alkalické taveniny na něj působí velmi slabě.
Tajemství stability tantalového kovu spočívá v tom, že na jeho povrchu je vždy tenký, ale velmi pevný film oxidu Ta2O5. Pokud látka nebo sloučenina může interagovat s tímto filmem nebo proniknout do tohoto filmu, zničí kov, a pokud ne, pak si tantal zachová svou „nenapustnost“. Mezi činidla s destruktivními vlastnostmi patří: ionty fluoru, oxid síry (VI) a dokonce i alkalické taveniny. Stejný film zabraňuje toku elektrického proudu z kovu do roztoku během elektrolýzy (kdy tantalová elektroda slouží jako anoda). Proto se tantal používá v elektronické technologii pro výrobu proudových usměrňovačů.
V nepřítomnosti kyslíku a dusíku je tantal odolný vůči mnoha tekutým kovům. Odkysličený kovový sodík na něj nemá vliv ani při 1200°C, hořčík a slitiny - uran-hořčík a plutonium-hořčík - při 1150°C. To umožňuje použití tantalu k výrobě některých částí jaderných reaktorů.
Tantal je schopen absorbovat poměrně významné množství (až 1 %) vodíku, kyslíku a dusíku. Dochází k procesu zvanému absorpce - jev absorpce látky celým objemem absorbéru bez vzniku silných sloučenin. Tento proces je reverzibilní. Když se kov zahřeje ve vakuu na 600 °C, absorbovaný vodík se úplně uvolní. Kov, který se stal křehkým vodíkem, získává své dřívější mechanické vlastnosti. Vlastnost tantalu rozpouštět plyny se využívá, když se přidává jako přísada do oceli.
Na. Při zvýšených teplotách se tvoří sloučeniny. Při 500 °C mohou existovat hydridy Ta2H nebo TaH v závislosti na obsahu vodíku v kovu. Nad 600 - 700°C se při interakci s kyslíkem objevuje oxid Ta2O5, při přibližně stejné teplotě dochází k reakci s dusíkem - vzniká nitrid tantalu TaN. Uhlík se spojuje s tantalem při vysokých teplotách (1200-1400°C), čímž vzniká TaC - žáruvzdorný a tvrdý karbid.
V roztavených alkáliích se tantal oxiduje za vzniku solí kyseliny tantalové, které lze spíše považovat za směsné oxidy 4Na2O .
3Ta2O5 .
25H20; 4K2O .
3Ta2O5 .
16H20. Tantal se rozpouští v kyselině fluorovodíkové za vzniku fluoridových komplexů typu [TaF6]-, 2-, 3-. Protože jsou komplexy nestabilní a hydrolyzují, roztok obsahuje komplexy - produkty hydrolýzy [TaOF5]2-, 3-.
Jód
IOD (lat. Iodium), I je chemický prvek skupiny VII periodického systému Mendělejeva, patří mezi halogeny (symbol J se vyskytuje i v literatuře); atomové číslo 53, atomová hmotnost 126, ...